强迫症(OCD)在世界范围终身患病率可高达3%,其病因复杂且病理不清,影响因素可包含环境和基因。现阶段强迫症发病机理研究难点之一就是:两者间是通过什么途径相关联从而导致疾病的产生?
越来越多的研究开始证明超罕见但可能具有高外显率的突变,可能是精神疾病发病机制的一个重要因素。近日,上海交通大学bat365中文官方网站林关宁教授团队与上海交通大学医学院附属精神卫生中心王振主任医师团队组合作对强迫症进行了核心家系(强迫症患者及其健康父母)队列的全基因组的研究,是国际上首个从全基因组层面分辨超罕见的OCD突变来研究强迫症病因,也是国际上首次提出除了常被研究的神经突触能与OCD发病机制相关外,表观遗传中的染色质修饰的失调,特别是组蛋白修饰的异常在OCD的疾病发展中也起到非常重要的作用。该研究把表观遗传学紊乱作为环境因素与遗传因素相互作用所在通路对未来研究具有很重要的提示作用。
研究人员首先通过对53个核心家系进行了全基因组测序,全面获取了强迫症患者及其健康父母所携带的所有基因变异,从中筛选出只存在于患者的超罕见的新发突变(de novo mutation)。发现了有24个单点以及一个大片段缺失的突变严重影响了蛋白质结构,而被这些突变影响的蛋白质在人脑中主要起到调节染色体结构的作用(图1A)。同时研究人员也发现很多非编码的新发突变也显著聚集在了染色体上具有关键功能的结构和区域上。
当研究人员进一步使用人脑表达数据构建了胚胎期与出生后的脑基因互作网络,发现上述突变所在基因集中在一个具有“染色质调控”作用的生物子网络中,该子网络与许多神经递质相关基因有很强的关联。因此,研究者推断基因突变导致染色体结构异常是强迫症的遗传病理机制中的关键一环,而这一异常可能是通过影响下游神经递质表达量而发挥作用(图1B-2)。研究结果不仅证实了超罕见突变(新发严重突变 damaging de novo mutation)对强迫症的发病可能有着显著的作用,还提示这些突变所造成的染色质结构调控的异常将可能是强迫症病理过程中的重要因素。
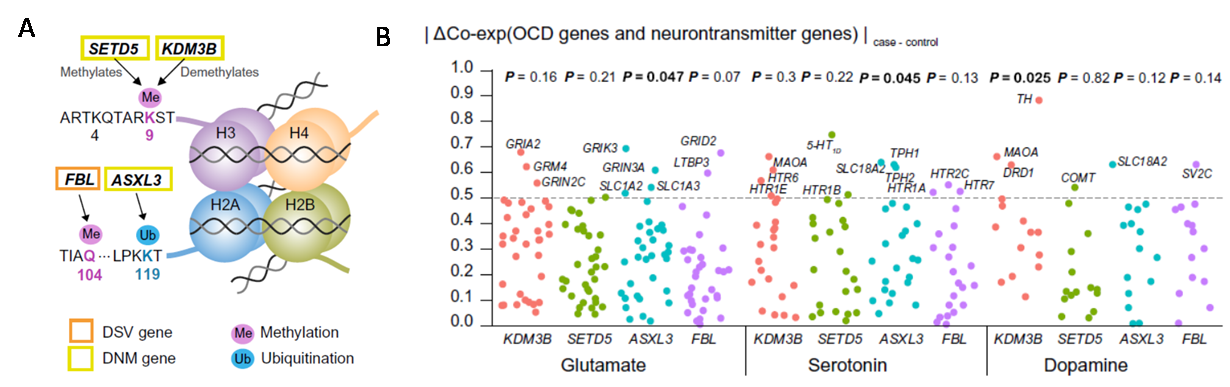
图1.全基因组家系研究发现的OCD关键突变基因及它们可能影响的神经递质系统基因
另外,此项研究还发现大约一半的患者携带至少一个严重的新发突变,也为此前悬而未决的强迫症“新发突变假说”提供了新的证据。以往有观点认为,对强迫症的遗传基础进行研究长期遇到困难是因为大部分致病突变都是在患者身上新发生的,且没有再遗传给后代就直接被自然选择淘汰了。然而,针对常见变异的全基因组关联分析以及针对来自先祖的罕见遗传变异的复杂家系研究都发现了一些致病遗传因素,因此有学者对“新发突变假说”抱有怀疑态度。本研究证实了导致强迫症发病的遗传因素确实有很大一部分是由新发突变构成的,这为“新发突变假说”提供了新的支持证据,也为既往强迫症遗传研究遇到的瓶颈提供了新的解决路径。这一发现获得的OCD致病突变及所揭示的疾病通路可作为病理和药物研究靶向。
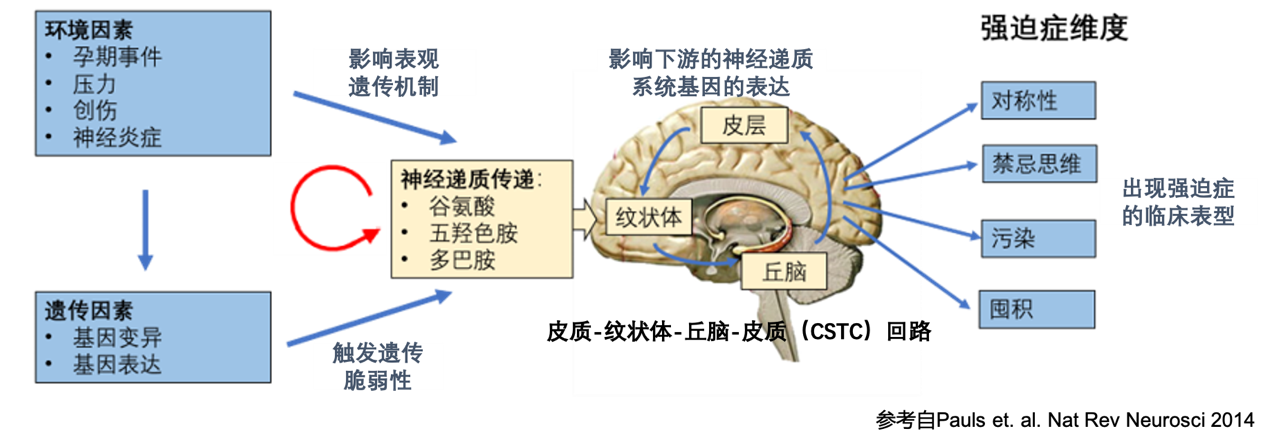
图2. 基于环境因素和基因风险交互影响的OCD表观遗传的发病机制假设
此外,通过将强迫症基因与抽动症基因进行比较分析,研究人员还发现了一个有趣的结果:这是两种临床表型具有一定相似性的精神疾病,虽然它们的致病基因具有高度相似的底层生物学功能,但研究人员发现两疾病的基因却表达在不同的脑发育阶段、或脑区与脑细胞类型中。这一结果可说明,强迫症与抽动症可能是具有同一病理过程,但发生在不同时空位点而形成的两种临床表型交叉的疾病。
相关论文“De novo mutations identified by whole-genome sequencing implicate chromatin modifications in obsessive-compulsive disorder”于1月12号被《Science Advances》在线刊登。上海交通大学医学院附属精神卫生中心王振主任医师、上海交通大学bat365中文官方网站林关宁教授为共同通讯作者。第一作者为上海交通大学bat365中文官方网站林关宁教授,上海交通大学医学院附属精神卫生中心的博士研究生宋炜宸,助理研究员王卫娣,住院医师王佩,为论文共同第一作者。该项研究得到国家自然科学基金、上海市自然科学基金、上海市教委科研创新计划、上海市卫生健康委员会等项目的资助。